Insulina inalável: afinal, foi ou não aprovada?
Há muita gente falando que uma versão inalável de insulina, chamada Afrezza, foi aprovada nos EUA. Entenda por que isto é uma meia-verdade e saiba o que podemos esperar do futuro.
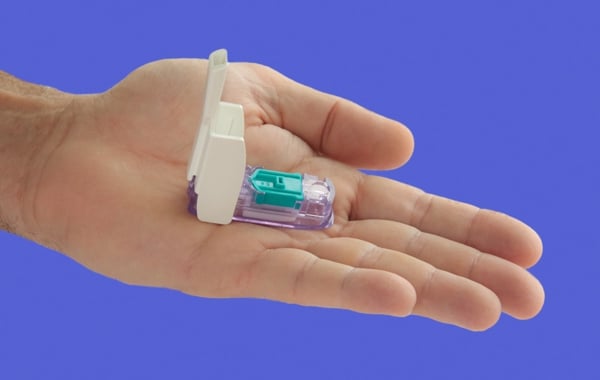
Para quem precisa injetar diariamente insulina, ouvir a notícia de que, em breve, haverá uma versão inalável do hormônio parece ser boa demais para ser verdade. Já pensou poder se livrar para sempre das injeções e, ao invés, apenas “respirar” insulina?
Na semana passada, o mundo do diabetes entrou em polvorosa quando um painel de especialistas da FDA (a “ANVISA” dos EUA, órgão que regula a venda de medicamentos) aprovou, com 13 votos a favor e apenas 1 contra, a comercialização da insulina inalável Afrezza, da farmacêutica MannKind.
Muitos sites e blogs chegaram a divulgar que a Afrezza havia sido aprovada pela FDA, e que portanto iria chegar em pouco tempo às prateleiras das farmácias. Isto, infelizmente, está longe da verdade. O que aconteceu foi que o painel de especialistas aprovou a liberação do novo medicamento; faltava ainda a FDA acatar à decisão dos consultores.
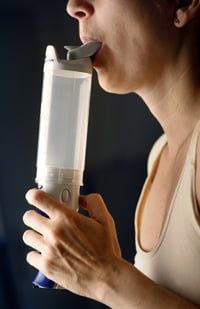
O CASO DE FRACASSO DA PRIMEIRA INSULINA INALÁVEL
Esta é a segunda vez que uma insulina produzida para ser inalada foi liberada para o público.
A primeira se chamava Exubera, mas ela sumiu do mercado em 2010 por medo de que pudesse causar danos aos pulmões.
Na época, os dados do último teste clínico da Exubera (que mostraram que 6 dos 4.740 pacientes que testaram o medicamento desenvolveram câncer nos pulmões) levantaram dúvidas quanto à segurança do medicamento.
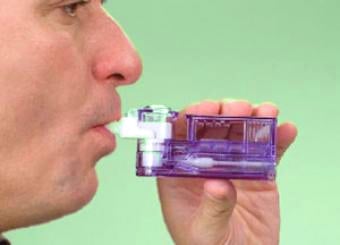
Além disso, o aparelho inalador, em si, era gigantesco (veja na foto à direita) e não fez sucesso entre o público diabético.
NEM TUDO ESTÁ BEM COM A AFREZZA
O medo de que insulinas inaláveis possam causar câncer de pulmão foi o que levou um dos membros do painel de avaliação a votar contra a liberação da Afrezza. Além disso, o membro afirmou que não há dados que comprovem que a insulina inalável é tão efetiva quanto as versões injetáveis.
Talvez esta opinião tenha tido mais peso para o órgão regulatório do que as outras 13. Nesta segunda-feira, a FDA, que historicamente segue o que os especialistas sugerem, divulgou uma nota na qual afirma que vai analisar até o dia 15 de julho se libera ou não a Afrezza.
Durante este tempo, a FDA irá reavaliar todos os testes clínicos feitos pela Mannkind sobre a eficiência e segurança da nova insulina inalável.
No mesmo dia do anúncio, as ações da farmacêutica despencaram. A empresa perdeu 16% de seu valor de mercado em menos de 24 horas.
Resta aos diabéticos, agora, torcer para que até meados de julho a agência regulatória dos EUA decida-se definitivamente pela liberação ou não da Afrezza. Principalmente, torçamos para que esta nova insulina inalável, que é um sonho para muita gente, seja mesmo eficaz e ajude-nos a cuidar melhor da nossa glicemia.
Remissão do diabetes tipo 2 é uma realidade cada vez mais frequente, afirmam entidades médicas
Um dos termos mais procurados junto com “diabetes” é “cura“. Afina…